2020年浙江高考化学答案解析
1.水溶液呈酸性的是( )
答案:B
3.下列物质在熔融状态下不导电的是( )
答案:C
4.下列物质对应的组成不正确的是( )
答案:B
5.下列表示不正确的是( )
答案:B
6.下列说法不正确的是(
答案:C
7.下列说法正确的是( )
答案:D
8.下列说法不正确的是( )
答案:B
9.下列说法不正确的是( )
答案:D
10.反应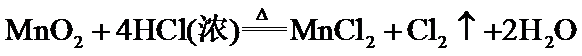 中,氧化产物与还原产物的物质的量之比是( )
中,氧化产物与还原产物的物质的量之比是( )
答案:B
11.下列有关实验说法不正确的是( )
答案:A
12.下列说法正确的是( )
答案:A
14.下列说法不正确的是()
答案:A
15.有关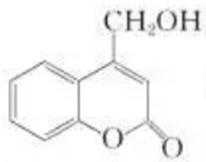 的说法正确的是( )
的说法正确的是( )
答案:A
17.下列说法不正确的是( )
答案:A
18.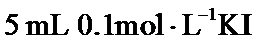 溶液与
溶液与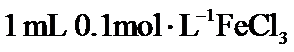 溶液发生反应:
溶液发生反应: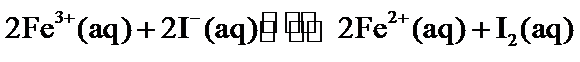 ,达到平衡。下列说法不正确的是( )
,达到平衡。下列说法不正确的是( )
答案:D
19.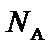 为阿伏加德罗常数的值。下列说法正确的是( )
为阿伏加德罗常数的值。下列说法正确的是( )
答案:A
20.一定条件下: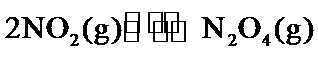
 。在测定
。在测定 的相对分子质量时,下列条件中,测定结果误差最小的是( )
的相对分子质量时,下列条件中,测定结果误差最小的是( )
答案:D
21.电解高浓度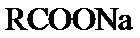 (羧酸钠)的
(羧酸钠)的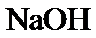 溶液,在阳极
溶液,在阳极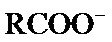 放电可得到
放电可得到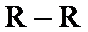 (烷烃)。下列说法不正确的是( )
(烷烃)。下列说法不正确的是( )
答案:A
22.关于下列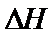 的判断正确的是( )
的判断正确的是( )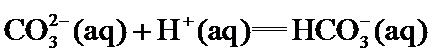
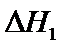
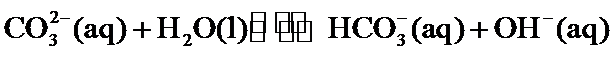
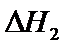
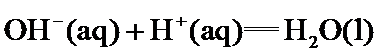
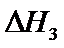
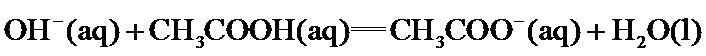
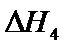
答案:B
23.常温下,用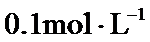 氨水滴定
氨水滴定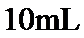 浓度均为
浓度均为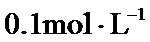 的
的 和
和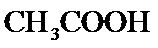 的混合液,下列说法不正确的是( )
的混合液,下列说法不正确的是( )
答案:D
24.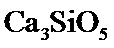 是硅酸盐水泥的重要成分之一,其相关性质的说法不正确的是( )
是硅酸盐水泥的重要成分之一,其相关性质的说法不正确的是( )
答案:D
25.黄色固体X,可能含有漂白粉、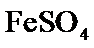 、
、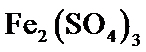 、
、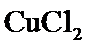 、
、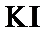 之中的几种或全部。将X与足量的水作用,得到深棕色固体混合物Y和无色碱性溶液Z。下列结论合理的是( )
之中的几种或全部。将X与足量的水作用,得到深棕色固体混合物Y和无色碱性溶液Z。下列结论合理的是( )
答案:C
26.(4分) (1)气态氢化物热稳定性 (2) (3)常温下,在水中的溶解度乙醇大于氯乙烷,原因是__________。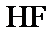 大于
大于 的主要原因是__________。
的主要原因是__________。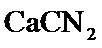 是离子化合物,各原子均满足8电子稳定结构,
是离子化合物,各原子均满足8电子稳定结构,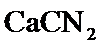 的电子式是_______。
的电子式是_______。
答案:
(1)原子半径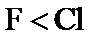 ,键能
,键能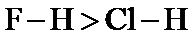 (2)
(2) (3)乙醇与水之间形成氢键而氯乙烷没有
(3)乙醇与水之间形成氢键而氯乙烷没有
Ⅰ.(1)
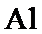 、
、
 (2)
(2)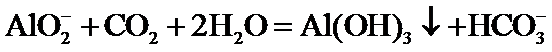 (3)
(3) 或
或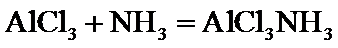 Ⅱ.(1)吸水或放热导致
Ⅱ.(1)吸水或放热导致 挥发
(2)
挥发
(2) 气体会将
气体会将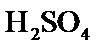 带出,与
带出,与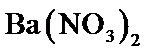 作用生成
作用生成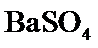
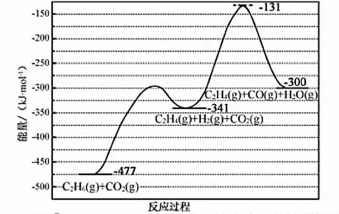
29.(10分)研究 相关的主要化学反应有: Ⅰ Ⅱ Ⅲ Ⅳ 已知: 可根据相关物质的相对能量计算反应或变化的 请回答: (1)①根据相关物质的相对能量计算 ②下列描述正确的是_____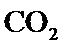 氧化
氧化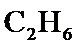 制
制 对资源综合利用有重要意义。
对资源综合利用有重要意义。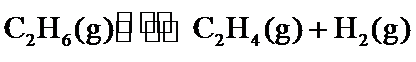
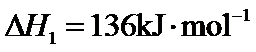
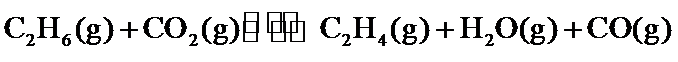
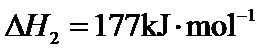
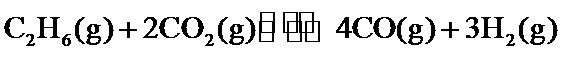
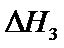
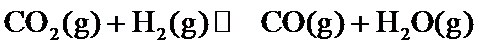
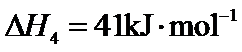
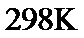 时,相关物质的相对能量(如图1)。
时,相关物质的相对能量(如图1)。
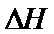 (
(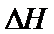 随温度变化可忽略)。例如:
随温度变化可忽略)。例如: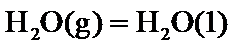
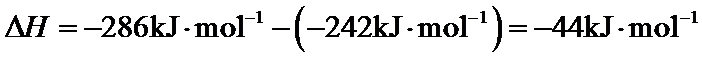 。
。 _____
_____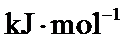 。
。
答案:
(1)①430 ②AD
③
 (2)①
(2)①
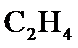 的产率低,说明催化剂X有利于提高反应Ⅲ速率
②选择性膜吸附
的产率低,说明催化剂X有利于提高反应Ⅲ速率
②选择性膜吸附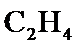 ,促进反应Ⅱ平衡正向移动
,促进反应Ⅱ平衡正向移动
30.(10分)硫代硫酸钠在纺织业等领域有广泛应用。某兴趣小组用下图装置制备 合成反应: 滴定反应: 已知: 实验步骤: Ⅰ. Ⅱ. 产品分离提纯:产品混合溶液经蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到 Ⅲ. 产品纯度测定:以淀粉作指示剂,用 请回答: (1)步骤Ⅰ 单向阀的作用是______;装置C中的反应混合溶液 (2)步骤Ⅱ 下列说法正确的是_____。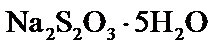 。
。
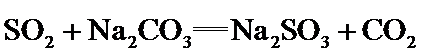
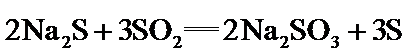
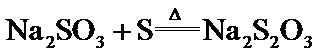
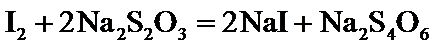
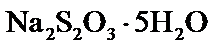 易溶于水,难溶于乙醇,
易溶于水,难溶于乙醇,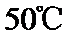 开始失结晶水。
开始失结晶水。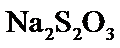 制备:装置A制备的
制备:装置A制备的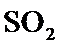 经过单向阀通入装置C中的混合溶液,加热、搅拌,至溶液
经过单向阀通入装置C中的混合溶液,加热、搅拌,至溶液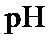 约为7时,停止通入
约为7时,停止通入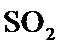 气体,得产品混合溶液。
气体,得产品混合溶液。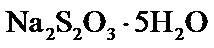 产品。
产品。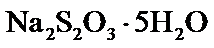 产品配制的溶液滴定碘标准溶液至滴定终点,计算
产品配制的溶液滴定碘标准溶液至滴定终点,计算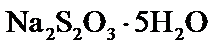 含量。
含量。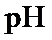 过高或过低将导致产率降低,原因是_______。
过高或过低将导致产率降低,原因是_______。
答案:
(1)防止倒吸
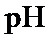 过高,
过高,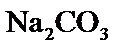 、
、 反应不充分;
反应不充分;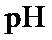 过低,导致
过低,导致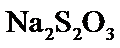 转化为S和
转化为S和 (2)BC
(3)①F、B、E、C、G ②防止碘挥发损失
③
(2)BC
(3)①F、B、E、C、G ②防止碘挥发损失
③ ;失去部分结晶水的
;失去部分结晶水的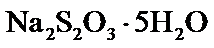
31.(12分)某研究小组以邻硝基甲苯为起始原料,按下列路线合成利尿药美托拉宗。 已知: 请回答: (1)下列说法正确的是________。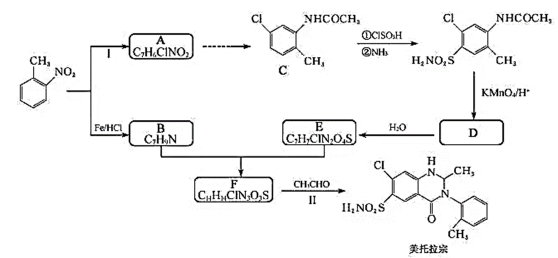
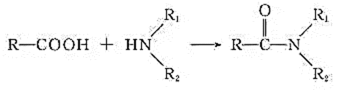
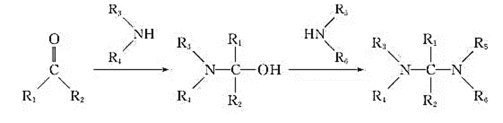
答案:
(1)BC
(2)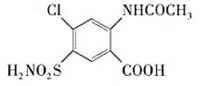 (3)
(3)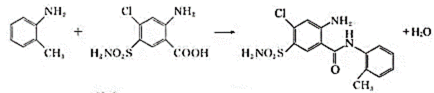 (4)
(4)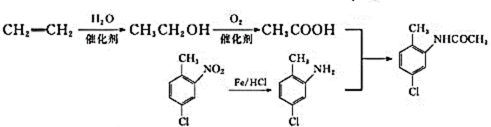 (5)
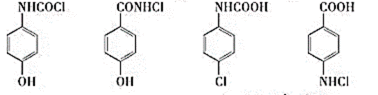
(5)


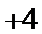 价,Y元素与Z、M元素相邻,且与M元素同主族;化合物
价,Y元素与Z、M元素相邻,且与M元素同主族;化合物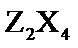 的电子总数为18个;Q元素的原子最外层电子数比次外层少一个电子。下列说法不正确的是( )
的电子总数为18个;Q元素的原子最外层电子数比次外层少一个电子。下列说法不正确的是( ) 溶液与
溶液与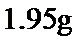 锌粉在量热计中充分反应。测得反应前温度为
锌粉在量热计中充分反应。测得反应前温度为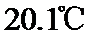 ,反应后最高温度为
,反应后最高温度为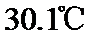 。
。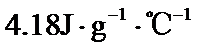 、溶液的密度均近似为
、溶液的密度均近似为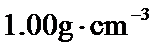 ,忽略溶液体积、质量变化和金属吸收的热量。请计算:
,忽略溶液体积、质量变化和金属吸收的热量。请计算: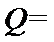 _____J。
_____J。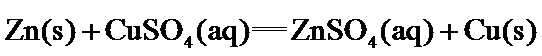 的
的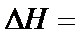 ______
______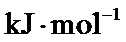 (列式计算)。
(列式计算)。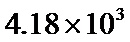 (2)
(2)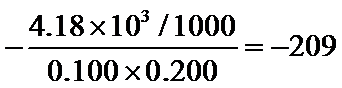
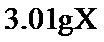 ,用含
,用含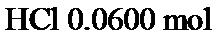 的盐酸完全溶解得溶液A,将溶液A分成
的盐酸完全溶解得溶液A,将溶液A分成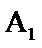 和
和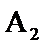 两等份,完成如下实验(白色沉淀C可溶于
两等份,完成如下实验(白色沉淀C可溶于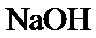 溶液):
溶液):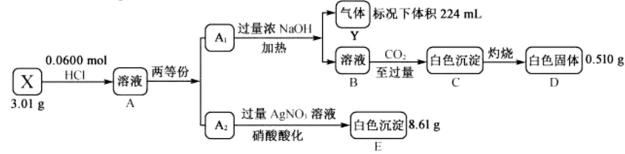
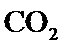 得到白色沉淀C的离子方程式是______________。
得到白色沉淀C的离子方程式是______________。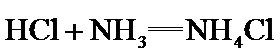 ”相同。
”相同。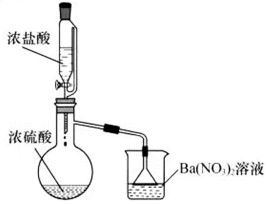
 气体的原因是_____________。
气体的原因是_____________。